“O药”国内获批胃癌适应症!六成患者多活2年!
 胃癌
|
阅读量:1802次
胃癌
|
阅读量:1802次
近日,纳武利尤单抗(欧狄沃,简称“O药”)正式获国家药品监督管理局(NMPA)批准,用于治疗既往接受过两种或以上全身性治疗方案的晚期或复发性胃腺癌或胃食管连接部腺癌患者。
提起大名鼎鼎的“O药”,全球肿瘤患者想必都不会陌生。它是一种作用于人程序性死亡受体-1(PD-1) 的阻断抗体,通过重新激活患者自身免疫细胞来杀伤肿瘤,是一种不同于传统化疗和靶向治疗的作用机制全新的抗肿瘤药物。
2018年6月,国家药监局便已批准O药用于治疗EGFR阴性、ALK阴性、既往接受过含铂方案化疗后疾病进展或不可耐受的局部晚期或转移性非小细胞肺癌成人患者。
2019年9月,O药又获批治疗接受含铂类方案治疗期间或之后出现疾病进展且肿瘤PD-L1表达阳性(定义为表达PD-L1的肿瘤细胞≥1%和≥2%)的复发性或转移性头颈部鳞状细胞癌患者。
此次是O药在国内获批的第3个适应症。据好医友统计,FDA已批准O药18个适应症,涉及9大癌种。期待O药能尽快在国内“解锁”更多适应症,造福中国癌友。
临床数据喜人!逾六成患者可多活2年
此次获批是基于一项Ⅲ期临床研究(ATTRACTION-2)。结果显示,纳武利尤单抗注射液用于胃癌三线或以上治疗安全性良好。
纳武利尤单抗治疗组达到完全缓解(CR)/部分缓解(PR)的患者,中位生存期达到了26.68个月,3年生存率仍有35.5%。这两个数字在晚期胃癌治疗中,是前所未有的。
在获益的患者中,有61.3%的人生存期可延长至2年以上。此外,该药还可显著降低51%的死亡风险,明确了其在晚期胃癌治疗领域的附加价值。而在该对照组实验中,O药的3-4级治疗相关不良事件发生率为10%。
值得一提的是,该研究首次明确了胃癌免疫治疗在东亚人群中的有效性及安全性,也使O药成为了首个经Ⅲ期临床研究证实,能为中国晚期胃癌患者带来显著生存获益的PD-1抑制剂。
真实案例
1名77岁的日本男子初诊胃癌后,接受了腹腔镜全胃切除术和淋巴结清扫术。首次手术的28个月后,腹部CT显示脾转移,遂行脾切除术。此后该患者进行了S-1联合奥沙利铂治疗,4个月CT复查提示肝内多发转移灶。后经二线治疗(雷莫芦单抗+紫杉醇)后,腹部CT显示肝转移灶进展。
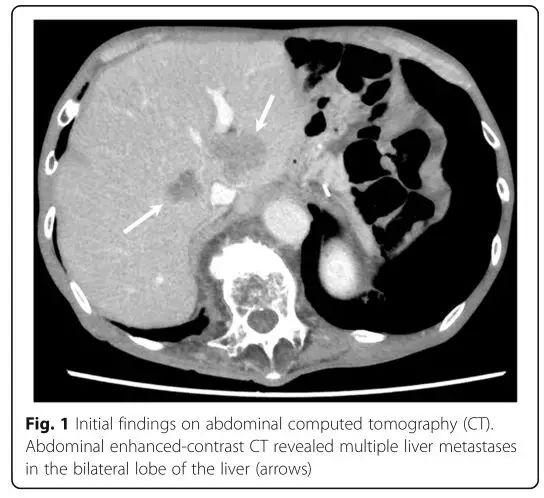
最终,患者的三线治疗选择了O药。4个周期治疗后,肝转移灶明显缩小,病灶较基线水平缩小55%,疗效达到部分缓解。8个周期后,病灶缩小了82.6%。12个周期后,腹部CT显示所有靶病灶全部消失,疗效评估为完全缓解。治疗过程中,患者没有出现任何不良反应(包括免疫相关不良反应)。患者继续使用O药治疗,用药8个月无疾病复发迹象。
这是首例文献报道的O药治疗达到完全缓解的胃癌患者。虽然非常罕见,但也表明了O药在成功治疗转移性胃癌方面的潜在价值。此前,已有许多国内胃癌患者通过好医友中美远程会诊受益于O药。
在中国,胃癌是仅次于肺癌的第二大癌种,其发病与死亡数均占全球约一半。约80%的中国胃癌患者确诊时已是晚期,可选治疗方案很有限且疗效局限。而O药作为第一个在中国获批用于胃癌治疗的免疫肿瘤药物,将改变中国胃癌后线治疗“无药可用”的现状。
想了解更多胃癌新疗法相关信息,欢迎后台留言或致电好医友(400-060-9693)。
2020-03-16 16:34

好医友小编
联系医学顾问
医学顾问微信在线
