晚期非小细胞肺癌患者,迎来一线免疫治疗新选择
 肺癌
|
阅读量:200次
肺癌
|
阅读量:200次
肺癌是全球癌症死亡的主要原因,约占所有癌症死亡人数的1/5。中国肺癌患者人数占全球肺癌患者总数的1/3以上。
肺癌通常分为非小细胞肺癌(NSCLC)和小细胞肺癌(SCLC),其中80-85%为NSCLC。
大部分NSCLC患者在确诊时已是晚期。
近日,美国FDA批准Libtayo与铂类化疗联用,一线治疗晚期非小细胞肺癌(NSCLC)成人患者。
这些患者必须是转移性或局部晚期肿瘤,不适合手术切除或化疗。无ALK、EGFR或ROS1突变,且不考虑PD-L1表达或组织学。
Libtayo(Cemiplimab rwlc)是一款PD-1抑制剂,通过阻断PD-1与其配体的结合,增强T淋巴细胞的抗癌免疫反应。
本此次批准是基于一项全球3期临床试验EMPOWER-Lung 3的结果,试验评估了Libtayo联合化疗与单独化疗的疗效。
共入组了466名局部晚期或转移性NSCLC患者,以2:1的比例随机分配。
该试验主要终点为总生存期(OS),次要终点包括无进展生存期(PFS)和总缓解率(ORR)。
结果显示:
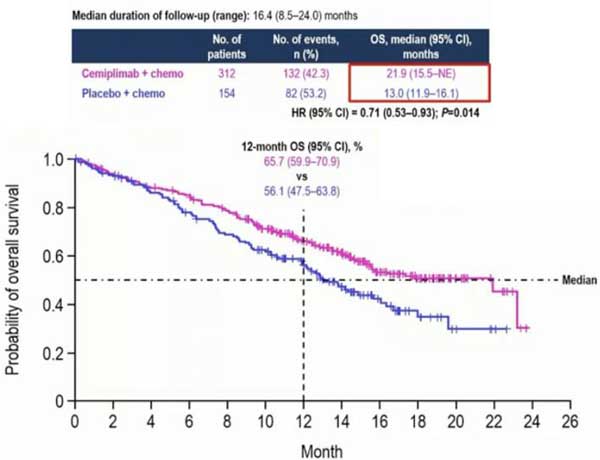
》 Libtayo组中位OS为21.9个月,单独化疗组为13.0个月,死亡风险降低了29%;
》 Libtayo组的12个月生存率为65.7%,单独化疗组为56.1%;
》 中位PFS方面,Libtayo组为8.2个月,单独化疗组为5.0个月;
》 ORR方面,Libtayo组为43%,单独化疗组为23%;
》 安全性方面,常见不良反应是脱发、恶心、疲劳等,未观察到新的安全信号。
好医友医疗网肺癌专家David Berz博士介绍:
此次批准让Libtayo有望成为晚期非小细胞肺癌关键治疗方案,既可作为PD-L1高表达者的单一疗法,也可与化疗联用,从而延长患者的生存期。
希望Libtayo的获批,能为患者带来更多新的治疗选择和临床获益。
参考来源:
https://www.pharmaceutical-technology.com/news/fda-regeneron-libtayo-chemotherapy/
2022-11-14 16:44

好医友小编
联系医学顾问
医学顾问微信在线
