胰腺癌的治疗:胰腺癌细胞是怎样逃过免疫“监视”的?
 医学资讯
|
阅读量:次
医学资讯
|
阅读量:次
近年来,以免疫检查点抑制剂为代表的免疫疗法彻底改变了癌症治疗格局。但在胰腺癌方面,免疫疗法似乎表现欠佳。
对此,纽约大学格罗斯曼医学院研究人员在《自然》上发文,揭示了胰腺癌细胞逃避免疫反应的机制:利用细胞自噬,限制其表面MHC I类分子数量,从而阻碍抗原的呈递。而通过药物或基因方法抑制该通路,可以逆转胰腺癌免疫逃逸。
◎ 胰腺癌是怎么逃过免疫监视的?
目前,癌症治疗面临的主要障碍是免疫逃逸,常见机制包括由MHC-1突变或杂合性丧失引起的抗原呈递受损。免疫治疗耐药可能与此有关。
MHC-I是一组在细胞表面显示特定蛋白质片段的蛋白质。免疫T细胞会忽略带有MHC-I标记的细胞,但它们会识别并攻击带有异常标记的细胞,比如被病毒感染的细胞、发生癌变的细胞等。
而胰腺癌细胞是这样逃避免疫“监视”的:
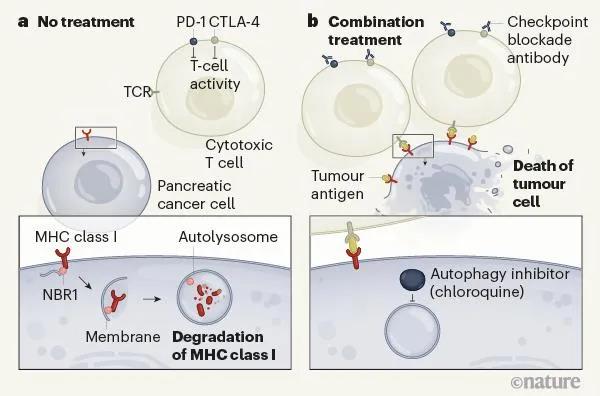
A.胰腺癌细胞通过“自噬”,破坏了MHC I类分子,从而阻止了它们从肿瘤中“呈递”抗原,逃过免疫系统识别。
B.在小鼠胰腺癌模型中,自噬抑制药物(氯喹)和PD-1、CTLA-4抑制剂联合治疗,激发了对肿瘤的强大免疫反应。
◎ 胰腺癌细胞的“自噬”
胰腺导管腺癌(PDAC)是胰腺癌的最常见形式,对包括免疫检查点抑制剂在内的大多数疗法都具有耐药性。尽管胰腺导管腺癌MHC-1表达下调,但很少发现引起MHC-1缺失的突变。
在胰腺癌细胞中,大多数MHC I类分子并不存在于细胞表面,而是被拉入癌细胞和癌细胞内的囊泡中,被自噬降解。自噬是一种重要的细胞降解途径,它通过回收细胞器和蛋白质来维持细胞的“适应性”。
通过去除MHC-I标签,自噬可使癌细胞不被免疫系统识别,并使其对免疫疗法产生抵抗。
研究团队发现在PDAC细胞中,MHC-1分子通过自噬相关受体NBR1的自噬依赖性机制,被溶酶体选择性靶向并降解。
不过,通过阻断基因或使用抗疟药物氯喹抑制自噬,能显著恢复胰腺癌细胞表面的MHC-I表达水平,改善抗原呈递,并抑制胰腺癌小鼠模型的肿瘤生长。
此外,通过消耗CD8+T细胞或降低MHC-1的细胞表面表达,能逆转自噬抑制带来的抗肿瘤作用。
如果进一步将针对自噬机制的靶向药或氯喹,与双重免疫疗法(PD-1+CTLA-4抑制剂)联用,能显著增强抗肿瘤免疫反应。
因此,自噬和溶酶体通过选择性靶向降解MHC-1来增强肿瘤免疫逃逸。针对自噬机制的靶向药物与双重免疫检查抑制剂结合,有望作为胰腺癌治疗新方案。
◎ 让免疫治疗更有效
此外,在胰腺癌细胞中发现的MHC-I内化引起的免疫治疗的耐药性,可能在非小细胞肺癌等其他癌症中也起作用。
此前对胰腺癌患者的临床试验表明,羟氯喹联合标准化疗可提高患者对化疗的反应和免疫治疗效果。
针对自噬机制新联合疗法的安全性和有效性,还有待临床试验进一步验证。
2020-09-02 16:45

好医友小编
联系医学顾问
医学顾问微信在线
