美国放宽癌症临床试验入组标准,这5类患者可以抢先用新药了
 医学资讯
|
阅读量:次
医学资讯
|
阅读量:次
不久前,一位72岁杭州老人去美国看病的经历引发热议。老人在美16个月,参加了多个新药临床试验,正是这些新药延续了他的生命。美国引领全球的新药临床试验,让许多治疗本已山穷水尽的晚期癌症患者迎来柳暗花明。
不过,美国新药临床试验对入组者要求严格,若不符合相应标准,就不能入组。设置这些标准,一方面是为了保证试验结果的真实可靠;另一方面也为了尽可能地保护入组的患者,因为临床试验也有一定风险。
但这样一来,部分患者可能因此与新的治疗希望失之交臂,而临床试验的结果则也可能无法全面反映最终接受试验药物的患者群体的治疗效果。
为此,近日,美国FDA发布了4份《癌症临床试验资格标准的指南》草案以及一份《关于青少年入组成人癌症临床试验的指南》正式文件。这意味着,一些此前无法入组临床试验的患者,终于也有望受益于新疗法了!
1)儿童患者入组成人癌症临床试验的最低年龄

草案解释了在成人癌症临床试验中应如何评估儿科配方,需考虑儿童患者的年龄、体重、生理条件和治疗需求。
支持将2~12岁儿童癌症患者纳入成人癌症临床试验。
2岁以下的儿童不应被纳入成人癌症临床试验,因为他们年龄太小,药物代谢酶系统和器官功能尚未发育成熟,种种可预期和未知的毒性对他们的潜在伤害更大。
对于部分过了新生儿期(出生后28天)的2岁以内婴儿,如果有望从试验药物中获益,也可以考虑入组成人癌症临床试验。但前提是必须经过FDA允许,并且仅限于极少数特殊病例。
此外,草案还提出了在对足够数量的成人患者进行评估,明确安全性和毒性数据后,也可考虑将儿童患者纳入早期试验。而对于后期试验,应综合考量相应疾病的生物学特征、试验目标以及相关药物的作用机制和安全状况的现有数据,调整最低入组年龄。
2)纳入HIV、乙肝或丙肝感染者

艾滋病病毒(HIV)和乙肝感染如今已可被长期有效管理,而丙肝目前已可治愈。但目前,将HIV、乙肝或丙肝感染者排除在癌症临床试验之外的情况仍很常见。
草案指出,在很多情况下,扩大癌症临床试验的入组资格,将HIV、乙肝或丙肝感染者纳入其实是合理的,并可能加速开发出针对这些伴有慢性感染的癌症患者的有效疗法。
在癌症临床试验中纳入这些患者,并将这些信息加入药物标签中,在临床实践中可指导更广泛的患者群体安全有效地使用这些药物。在入组HIV感染者时,标准中应重点评估患者的免疫功能以及对HIV的治疗;入组乙肝或丙肝患者时,应考虑肝脏相关检测数据以及乙肝、丙肝的治疗。
3)纳入器官功能障碍者、患有第二原发癌或有既往史者
草案指出,将有严重器官功能(重点关注肾、心和肝功能)障碍者以及既往或同时患有其他原发癌症的患者排除在临床试验外,可能导致临床试验更倾向于招募年轻患者,这可能无法全面地代表该药物的潜在患者群体。
例如,在初始剂量发现或初步活性评估或概念验证性研究中,不应排除有第二原发癌或有既往史的患者。
4)纳入癌症脑转移患者
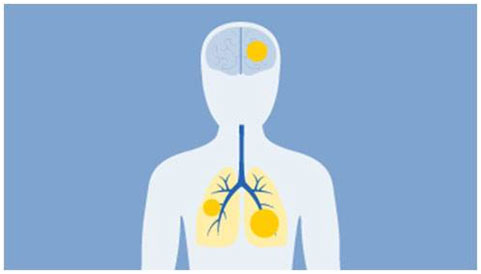
部分恶性肿瘤,如黑色素瘤、肺癌、乳腺癌的脑转移越来越常见。美国约有7万名癌症脑转移患者。然而,由于担心患者功能状态不佳、预期寿命缩短或毒性风险增加,癌症脑转移患者历来被排除在临床试验之外。
草案提出应将这些患者纳入临床试验,以便在保护患者安全的前提下,更好地了解试验药物的疗效和安全性。
草案解释了如何将癌症脑转移患者纳入早期阶段的临床试验,可以是在单独的队列中,可以是在计划子集分析队列中,以便更好地评估药物在脑转移患者中的初步疗效和安全性。
如果有充分的理由需要排除某些脑转移患者,则应在临床试验方案中加以说明。
5)青少年患者入组成人癌症临床试验
这份正式文件为青少年患者入组成人癌症临床试验提供了相应的建议,包括:入组标准、剂量和药代动力学评估、安全监测和伦理要求。
只有在获得初步的成人药代动力学和毒性数据后,青少年患者才可以参加首次人体试验或剂量递增试验。此外,只有那些复发/难治性青少年癌症患者,或没有可用的治疗标准药物时,才可以入组早期试验。
需要注意的是,前4份文件目前还只是草案,是由FDA根据美国临床肿瘤学会(ASCO)和癌症研究之友(FCR)的反馈意见所编写,还将参照公众意见进行审议、修订,不久后将会发布正式文件。
相信在不久的将来,越来越多国内患者也将能有机会获益于临床试验。
如需咨询更多美国临床试验相关信息,欢迎后台留言或致电好医友(400-060-9693)。
2019-03-18 16:58

好医友小编
联系医学顾问
医学顾问微信在线
