58%患者持续缓解超2年!罕见恶性肉瘤,迎来首款创新疗法
 软组织肉瘤
|
阅读量:200次
软组织肉瘤
|
阅读量:200次
近日,美国FDA批准mTOR抑制剂Fyarro(西罗莫司蛋白结合颗粒)注射用混悬液,用于治疗局部晚期、不可切除或转移性恶性血管周围上皮样细胞瘤(PEComa)的成年患者。
Fyarro是首个获得FDA批准治疗晚期恶性PEComa患者的疗法,同时也是这类罕见肉瘤的唯一疗法。
01/ 罕见恶性肉瘤,迎来新疗法
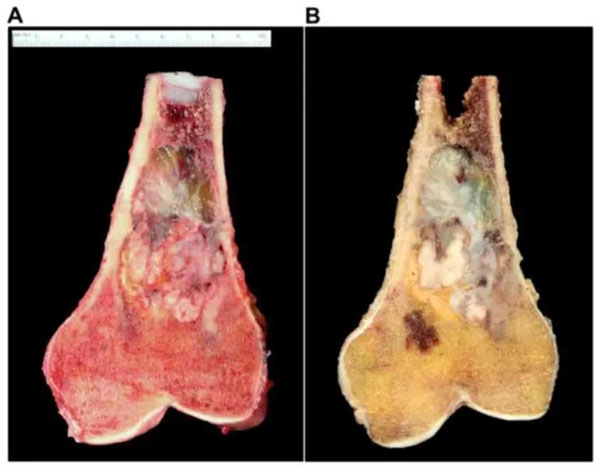
根据世界卫生组织(WHO)的定义,晚期恶性血管周围上皮样细胞肿瘤(PEComa)是由与血管壁关联的独特细胞组成的间充质肿瘤,通常同时表达黑色素细胞和平滑肌标志物。
PEComa是软组织肉瘤中的一个罕见亚型。在美国,每年约有100-300名新确诊患者。
恶性PEComas几乎可以发生在任何身体部位,通常是子宫、腹膜后、肺、肾、肝、泌尿生殖道和胃肠道,女性患者居多。
并且,该病的临床病程进展具有侵袭性,包括远处转移和最终死亡。据一项回顾性研究统计,PEComa患者的预后较差,生存期为12-16个月。
目前,PEComa尚无获批的疗法,主要通过手术治疗,常规化疗临床获益较小,而无法手术或转移性患者缺乏有效治疗手段,亟需更好的疗法。
02/ mTOR抑制剂:Fyarro
目前,已有证据显示,恶性PEComas主要是由于TSC1/TSC2基因发生突变,导致mTOR通路的激活,促使肿瘤生长。
TSC1/TSC2在多种实体瘤中广泛存在,包括肝癌、乳腺癌、膀胱癌、肾癌等。TSC1/TSC2是mTOR信号通路的重要负调控因子,也已经成为这类肿瘤治疗的热门靶点。
Fyarro(ABI-009)是西罗莫司(Sirolimus)白蛋白结合型纳米颗粒注射用混悬液,西罗莫司是一种mTOR抑制剂。
与目前已上市的一代和二代mTOR抑制剂相比,Fyarro的疗效和安全性更优,靶细胞抑制作用更强,潜力也更大。
此前,该药已被FDA授予孤儿药资格、快速通道资格和突破性疗法认定。
03/ 58%的患者持续缓解超2年,罕见肉瘤迎来首个疗法!

这一批准是基于2期AMPECT试验的积极数据,该研究评估了Fyarro单药治疗晚期恶性PEComa患者的疗效和安全性。
结果显示:
Fyarro单药治疗的总缓解率(ORR)为39%;其中,2名患者在长期随访中显示达到完全反应。
在获得缓解的患者中,92%的患者持续缓解时间≥6个月,67%的患者持续缓解时间≥12个月,58%的患者缓解持续时间≥2年。
目前,患者的中位无进展生存期(PFS)为8.9个月,中位缓解持续时间尚未达到。
Fyarro的安全性与其他mTOR类的疗法一致,未观察到新的安全信号。
局部晚期或转移性PEComa的患者迫切需要新的治疗方案。而创新mTOR抑制剂Fyarro,在这类患者中表现出持久的缓解,且安全性可控。并且,该药的上市,为这一罕见肉瘤的治疗带来了唯一的一种治疗选择。
2021-11-29 11:59

好医友小编
联系医学顾问
医学顾问微信在线
