卵巢癌铂耐药怎么办?新型抗体偶联药获批在望
 卵巢癌
|
阅读量:200次
卵巢癌
|
阅读量:200次
卵巢癌被称为“沉默的杀手”,是妇科恶性肿瘤中最凶险、最难治的肿瘤之一。卵巢癌在我国也是发病率较高的妇科肿瘤,每年新发患者超过5.5万例。
临床上,大部分卵巢癌患者会面临复发或铂类化疗耐药的问题。此类患者的预后较差,客观缓解率仅4%~13%,并且毒性很大。目前,这些患者缺乏有效的挽救化疗方案及靶向治疗药物,亟需新的治疗选择。
近日,美国FDA已接受抗体偶联药物(ADC)Mirvetuximab Soravtansine的生物制品许可申请,用于单药治疗叶酸受体α(FRα)高表达的铂耐药卵巢癌患者。

FRα是叶酸受体家族的一员,在上皮卵巢癌和三阴性乳腺癌中高表达。FRα介导的信号通路能影响肿瘤细胞的分裂和转移,因此抑制FRα可产生一定的直接抗癌活性。
Mirvetuximab是一种由FRα结合抗体、可裂解连接物和Maytansinoid有效载荷DM4组成的第一类ADC,可靶向灭杀癌细胞。该药在铂类化疗耐药的卵巢癌患者中表现出了良好的活性。
该申请是基于一项关键性3期临床试验的结果,入组了106例FRα高表达的铂耐药卵巢癌患者。
主要终点为客观缓解率(ORR),次要终点包括缓解持续时间 (DOR)、无进展生存期 (PFS)和安全性等。
▌结果显示:
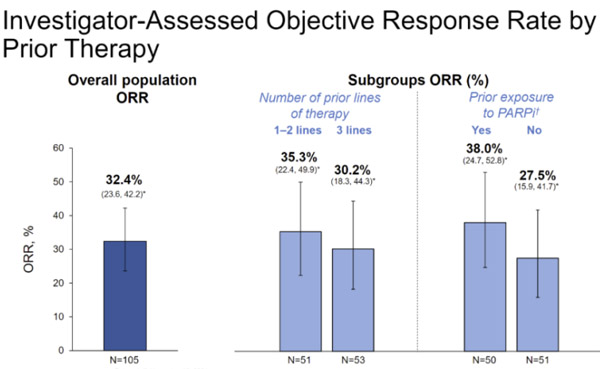
· 确认的ORR为32.4%,包括5例完全缓解,29例部分缓解。
· 中位DOR为6.9个月,无进展生存期为4.3个月。
· 在先前接受PARP抑制剂治疗的患者中,ORR为38%,DOR为5.7个月。
· 在未接受PARP抑制剂治疗的患者中,ORR为27.5%,DOR为5.9个月。
· Mirvetuximab的安全性良好,与之前的研究结果一致。
Mirvetuximab的国际多中心随机对照III期研究试验正在招募患者,这是一项旨在将加速批准转化为完全批准的确认性试验,预计将于2023年初公布该研究的关键数据。
好医友医疗网女性肿瘤专家Linnea Chap博士表示,FDA授予Mirvetuximab的优先审评资格证明了其治疗潜力,有望成为FRα高表达、对含铂疗法耐药的卵巢癌新标准疗法。
参考来源:
https://www.empr.com/home/news/drugs-in-the-pipeline/mirvetuximab-soravtansine-granted-priority-review-for-ovarian-cancer/
2022-05-31 15:47

好医友小编
联系医学顾问
医学顾问微信在线
