介入放射疗法治疗肝癌获批,它会是抗癌“神器”吗?
 肝癌
|
阅读量:200次
肝癌
|
阅读量:200次
“全国爱肝日”刚过不久,据世界卫生组织最新数据,肝癌是全球第六大癌症、中国第五大癌症,也是死亡率第三的癌症,全球一半以上新发和死亡肝癌病例都在中国。
由于肝癌恶性程度高且早期症状不明显,很多人一确诊就是中晚期,预后很差。中晚期肝癌难道真的没有希望了吗?
好消息是,最近,美国FDA批准TheraSphere钇-90微球疗法,用于治疗肝细胞癌(HCC,最常见的肝癌)患者。该疗法是美国批准的首个也是目前唯一一个用于治疗晚期肝细胞癌的介入放射疗法。

▌钇-90微球:中晚期肝癌治疗“利器”
好医友医疗网肿瘤精准医学专家迈克尔·卡斯特罗博士(曾多次获评“美国顶级医生”)介绍,目前,晚期肝癌虽不可治愈但仍可治疗。
肝癌常见治疗手段主要包括:外科治疗(手术切除、肝移植)、放疗、化疗、介入治疗(包括:介入化疗,介入放疗),以及靶向治疗、免疫治疗等。
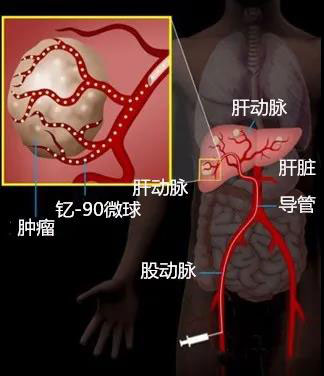
钇-90微球疗法是一种低毒性的选择性介入放射治疗(SIRT)方法,它包含数百万个含有放射性元素钇(Y-90)的微球,通过肝动脉导管直接输送到肝脏肿瘤中,精准释放β射线,而健康肝脏组织会通过门静脉获得血液,因此治疗过程中可最大程度减少对周围健康组织的损伤。
此次批准是基于一项名为LEGACY的临床研究的结果,旨在评估钇-90微球疗法治疗早期和晚期肝细胞癌的安全性和有效性。该研究分析了162名患者的数据,达到了客观缓解率和持续缓解时间两个主要终点(分别为4周72.2%和6个月76.1%)。
经过两次治疗后,患者完全或部分缓解——所有病灶消失或目标病灶直径缩小30%,接受移植或手术治疗的患者三年总生存率为93%。
研究发现,肝癌患者表现出非常高的应答率,且生存期显著延长,建议将其作为肝癌患者群的标准疗法。该研究结果已发表于《肝脏病学》杂志,可为临床医生提供决策依据。
采用TheraSphere钇-90疗法治疗无需住院,门诊就可进行,一般1小时内就能完成,可缓解医疗资源压力,特别是在疫情阴影之下。英国国家健康与医疗卓越研究所(NICE)发布的新指南认可了SIRT对患者和医院的益处,该指南建议将TheraSphere钇-90疗法治疗肝细胞癌纳入英国国家健康服务体系(NHS)。
钇-90疗法在改善肝细胞癌患者生存率和生活质量方面的益处,已经过20年的临床试验和全球7万多名患者的真实世界研究数据的证明。美国FDA的批准和英国NICE的建议,有望进一步促进该疗法的普及。
据悉,研究者计划启动一项临床试验,研究TheraSphere钇-90疗法+免疫疗法联合治疗,在不符合治疗条件的肝细胞癌患者中的疗效。此外,还将在其他癌种(包括前列腺癌和脑癌)中开展相关研究。
▌钇-90疗法并非“神器”
据了解,目前全球共有两款钇-90微球疗法已获得临床应用:TheraSphere(玻璃微球)和SirSphere(树脂微球)。其中,后者2002年获FDA批准用于结直肠癌,已在国内提交上市申请。
卡斯特罗博士提醒,钇-90微球疗法也不应神化,需充分考虑其适应症,评估患者的肝功能和身体状况,同时也要警惕和应对并发症。
鉴于肝癌的复杂性,多学科协助诊疗模式(MDT)至关重要。晚期肝癌患者在尝试新疗法前,应请多学科专家团队共同制定最适合的个性化综合诊疗方案。
▌肝癌治疗有哪些新进展?
钇-90微球疗法属于局部治疗,对于肝癌全身治疗,近年来也有不少新进展,尤其是靶向治疗和免疫治疗方面,新疗法让许多患者延长了生存期,提高了生活质量。
◆ 肝癌靶向疗法:
◎ 一线靶向药
2005年,抗血管生成药物索拉非尼获FDA批准上市,是首个肝癌靶向药物。
2018年8月,FDA批准仑伐替尼上市,用于一线治疗无法切除的肝细胞癌。同年9月,仑伐替尼进入中国。2020年新版《医保药品目录》中,仑伐替尼医保降价幅度高达80.7%,极大减轻了中国肝癌患者的用药负担。
◎ 二线靶向药
2017年,瑞戈非尼获FDA批准,用于索拉非尼耐药的晚期肝细胞癌患者。目前,该药已进入我国医保,降幅比例达45.56%。
2018年,FDA批准卡博替尼上市,用于治疗接受过索拉非尼或其他标准全身治疗后进展的晚期肝细胞癌患者。
2019年5月,雷莫芦单抗获FDA批准,二线单药治疗甲胎蛋白(AFP)≥400ng/ ML、索拉非尼耐药的肝癌患者。
◆ 肝癌免疫疗法:
◎ 单药免疫治疗
2017年,FDA批准“O药”纳武利尤单抗上市,用于既往用索拉非尼治疗过的肝癌患者(二线治疗),这是首个获批治疗肝癌的免疫检查点抑制剂,打破了长久以来肝癌治疗手段的局限。
2018年,“K药”帕博利珠单抗获批新适应症,用于先前已接受索拉非尼治疗的肝细胞癌患者(二线治疗)。
2020年3月,PD-1抑制剂卡瑞利珠单抗获国家药监局批准,用于治疗接受过索拉非尼和/或含奥沙利铂系统化疗的晚期肝细胞癌患者。这是中国首个获批的肝癌免疫治疗药物。该药目前已纳入医保,降价幅度达八成。
◎ 免疫联合治疗
2020年3月,FDA批准纳武利尤单抗与CTLA-4抑制剂伊匹木单抗联用(O+Y),治疗既往接受过索拉非尼治疗的肝细胞癌患者。这是FDA批准的首个双重免疫疗法。
2020年5月,FDA批准抗PD-L1疗法“T药”阿替利珠单抗联合贝伐珠单抗(T+A),一线治疗不可切除性肝细胞癌患者。该联合疗法是首个获批用于治疗不可切除性肝癌的免疫治疗方案,目前已在中国获批,已成为不能手术的、肝功能较好的肝细胞癌患者首选用药。
此外,“D+T”双免疫疗法、帕博利珠单抗+仑伐替尼、新一代免疫免疫疗法M7824等新疗法,疗效也在临床试验中得到初步验证,期待这些药物能进一步提高肝癌患者的生存期。
遗憾的是,有些新疗法仅适合少数患者,有些尚未在国内上市。在尝试新疗法前,不妨先请国内外权威专家进行远程会诊,评估新疗法的适用性。
此外,对于部分治疗效果不佳的患者,不妨考虑入组国际前沿新疗法临床试验,将有望受益于全球前沿医疗成果。
2021-03-23 16:41

好医友小编
联系医学顾问
医学顾问微信在线
