肥大细胞增多症,迎来首款靶向疗法。持续缓解3年以上!
 其它
|
阅读量:200次
其它
|
阅读量:200次
近日,美国FDA宣布,批准阿伐替尼(Avapritinib,商品名:泰吉华Ayvakit)一项新适应症,用于治疗晚期全身性肥大细胞增多症(SM)成年患者,包括侵袭性SM(ASM)、伴有血液肿瘤的SM(SM-AHN)和肥大细胞白血病(MCL)。
这是晚期SM患者首次获批的靶向疗法,旨在有效和选择性抑制携带D816V突变的KIT酪氨酸激酶(该疾病的核心驱动因素)。
▌肥大细胞增多症(SM)
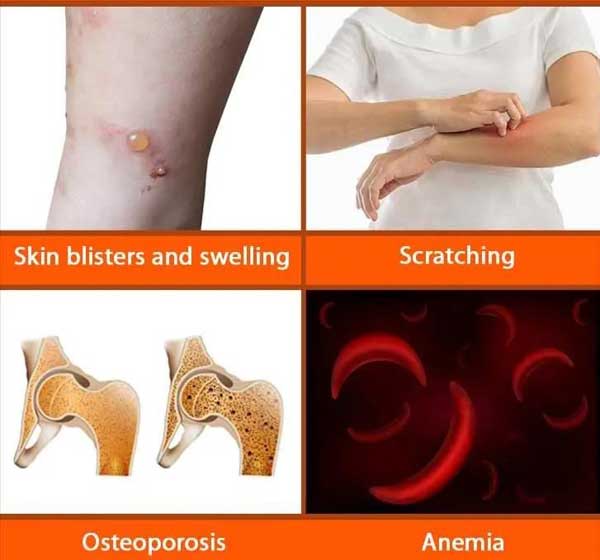
肥大细胞增多症(SM)是一种罕见的血液系统疾病,主要是由KITD 816V突变驱动。
肥大细胞不受控制的增殖和激活,会导致SM患者全身多器官系统发生广泛损伤。该病可发生在任何年龄,临床表现各不相同。
晚期SM亚型包括ASM、SM-AHN和MCL。其中,ASM患者的中位总生存期约为3.5年,SM-AHN约为2年,而MCL患者还不到半年。
即便采用了多种对症疗法,但过敏反应、斑丘疹、瘙痒、腹泻、脑雾、疲劳和骨痛等衰弱症状,仍在SM的所有类型中持续存在,导致患者的工作和日常活动受限,面临着身体和精神上的双重压力。
此前,尚无获批的疗法可以选择性地抑制KIT D816V突变,迫切需要新的治疗方案来解决这些危及生命的并发症。
▌广谱KIT/PDGFRA抑制剂:阿伐替尼
阿伐替尼是一种激酶抑制剂(KIT),可选择性和精准靶向抑制KIT 、PDGFRα突变激酶,具有广泛抑制作用。
目前,已获得FDA批准两种适应症:
① 携带PDGFRA外显子18的不可切除或转移性胃肠道间质瘤(GIST)成年患者,包括PDGFRA D842V突变。
② 晚期SM成人,包括ASM、SM-AHN和MCL,以及PDGFRα D842V。
今年3月,阿伐替尼获得我国国家药监局(NMPA)批准阿伐替尼的适应症为:用于治疗携带血小板衍生生长因子受体(PDGFRα)外显子18突变(包括PDGFRα D842V突变)的不可切除性或转移性GIST成年患者。
▌疗效持久,临床试验惊艳!
FDA的这一批准是基于1期EXPLORER试验和2期PATHFINDER试验的积极数据。
结果显示:
· 阿伐替尼在不同疾病亚型的晚期SM患者中显示出持久的临床疗效,且不论先前的治疗如何。
· 中位随访期11.6个月时,53例可评估患者中的总缓解率(ORR)为57%,完全缓解/血液学完全缓解率(CR/CRh)为28%。中位缓解持续时间长达三年多(38.3个月)。
需要注意的是,血小板计数低(低于50,000/μL)的晚期SM患者不推荐使用阿伐替尼。
晚期系统性肥大细胞增多症患者,通常会出现一些危及生命的并发症,或者改变他们日常活动能力的衰弱症状。
而阿伐替尼为SM患者带来了显著的临床获益,有望转变这一疾病的精准治疗模式,造福更多的SM患者。
2021-06-21 15:26

好医友小编
联系医学顾问
医学顾问微信在线
