用药半年,疗效显著!5年来,脂肪肝迎来首个突破性疗法
 其它
|
阅读量:215次
其它
|
阅读量:215次
说到脂肪肝,想必大家都不陌生:问问身边发福的亲友,看看每年的体检报告……
脂肪肝分为酒精性的和非酒精性(NAFLD,现更名为MAFLD,即代谢相关脂肪性肝病),后者主要由不良生活习惯引起,患病的人越来越多,每4个成年人中就有1个。如不加控制,NAFLD会发展为非酒精性脂肪性肝炎(NASH),进而引发肝癌。
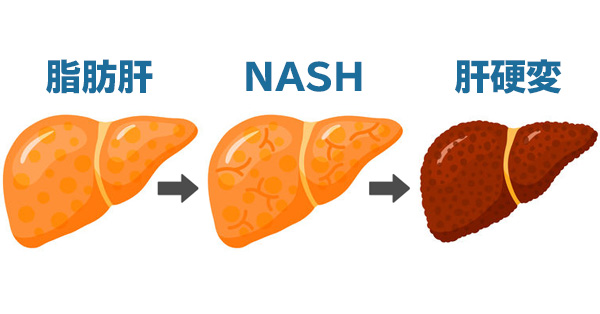
虽然存在大量临床需求,但NASH至今还没有新药上市。
好消息是:近日,美国FDA宣布,授予Lanifibranor“突破性疗法”认定,用于治疗NASH。这是自2015年1月以来,首个获此认定的NASH候选药物。
在为期24周的临床试验中,Lanifibranor达到了主要终点。在意向治疗人群(ITT)和符合方案人群(PPP)中,治疗组达到了脂肪变性活动度纤维化评分(SAF)统计学意义上的显著降低,且肝纤维化程度没有恶化。
NASH领域药物空白,亟待填补!
非酒精性脂肪性肝炎(NASH)是一种和人体代谢相关的疾病,表现为肝脏脂肪堆积,伴随炎症和细胞损伤。炎症可导致肝纤维化、肝硬化、门静脉高压症、肝癌,最终导致肝功能衰竭。

随着病毒性肝炎的有效防控,NASH现已成为新的肝癌威胁,影响全球2%~4%的人口。在美国,NASH已成为美国肝移植的第二大常见原因。而在中国,糖尿病和肥胖发病率的显著上升,使得NASH患病率居全球首位。
虽然目前针对NASH尚无获批的疗法。但NASH新药研发一直未曾中断。
NASH药物之所以研发难度大,主要是其致病机理太复杂,脂肪酸累积、胰岛素抵抗、免疫信号异常、炎症细胞和细胞凋亡等,都与之相关。因此,针对不同的靶点有不同的药物开发方向。
在NASH新药方面,在研FXR激动剂奥贝胆酸(Ocaliva)目前已被FDA授予突破性药物资格(BTD)。它也是全球第一个进入和成功完成III期临床的研究性药物。Ocaliva已于2016年5月在美获批上市,用于治疗原发性胆汁性胆管炎(PBC)。
目前,奥贝胆酸正被开发用于多种慢性肝脏疾病的治疗,包括NASH、原发性硬化性胆管炎、胆道闭锁等。不过,此前FDA拒绝了该药治疗NASH的新药上市申请,要求补充更多临床数据,说明它尚不足以成为一款理想的NASH药物。
创新PPAR激动剂:Lanifibranor
Lanifibranor是一种口服小分子泛PPAR激动剂,通过激活所有三种过氧化物酶体增殖物激活受体(PPAR)亚型来诱导体内抗纤维化,抗炎以及有益的血管和代谢变化。PPAR是一种特征良好的核受体蛋白,调节基因表达。
它能以一种均衡有效的方式靶向所有三种PPAR亚型,平衡激活PPARα和PPARδ,部分激活PPARγ。
Lanifibranor的特点决定了它有助于形成良好的耐受性,这在迄今为止的临床试验和临床前研究中均已被证实。
此前,Lanifibranor已获得了美国FDA和欧洲药品管理局(EMA)的“孤儿药”资格。
临床结果亮眼,肝脏改善明显!
此次认定是基于一项为期24周的随机、双盲、安慰剂对照的IIb期临床试验(NATIVE)的积极结果。该试验入组全球多个国家的247例NASH患者,评估Lanifibranor在改善肝脏炎症和肝细胞气球样变方面的疗效。
结果显示:
接受剂量为1200 mg/d的Lanifibranor治疗的意向治疗(ITT)患者群中,评估肝细胞炎症和肝细胞气球样变的SAF评分与基线相比显著降低。治疗组有49%的患者达到主要终点,安慰剂组为27%。
同时,也达到了多个关键次要终点,包括NASH消失且纤维化无恶化、肝脏纤维化改善且NASH无恶化。
根据这些积极结果,Lanifibranor是第一个在美国FDA和欧盟EMA两个监管的主要终点(NASH消失且纤维化无恶化,纤维化改善且NASH无恶化)上获得统计学显著结果的NASH候选药物。预计2021年上半年将进行III期临床试验。
在半年内就能取得如此喜人的疗效,Lanifibranor有望成为NASH领域的明星药物,让我们拭目以待!
2020-10-15 11:17

好医友小编
联系医学顾问
医学顾问微信在线
