疾病控制率100%,安全性良好!晚期非小细胞肺癌有望迎来靶向药
 医学资讯
|
阅读量:次
医学资讯
|
阅读量:次
近日举行的IASLC 2019世界肺癌大会(WCLC 2019)上,一项测试KRAS抑制剂AMG 510毒性的临床试验表明,在晚期非小细胞肺癌患者中,AMG 510对KRAS G12C突变患者显示出早期有潜力的抗肿瘤活性,且副作用很少。这项1期临床试验吸引了业界众多的关注,是本次大会最瞩目的研发项目之一。
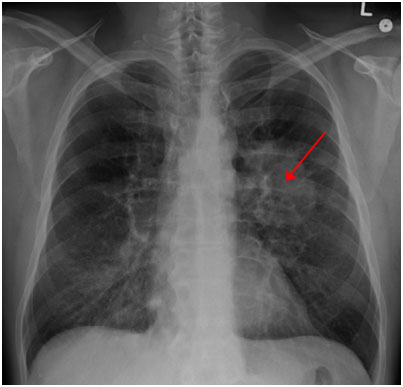
图示:胸片上可见肺癌。(来源:James Heilman医学博士/维基百科)
KRAS是一种鸟嘌呤核苷酸结合蛋白,在细胞内充当分子开关,与受体酪氨酸激酶激活和细胞内信号传导有关。KRAS G12C突变被认为是驱动肿瘤形成的一个致癌因素,这种突变存在于大约14%的肺腺癌患者和11%的非小细胞肺癌患者中。
KRAS突变被称为“最难对付的突变”,直接针对KRAS靶点原位研发药物难度很大。很多研究此前试图攻克这个堡垒,但都以失败告终。EGFR抑制剂都已开发到了第四代,但目前还没有针对这种突变获批的靶向方法。
为了测试AMG 510的安全性和毒性,圣路易斯华盛顿大学医学院Siteman癌症中心拉玛斯瓦米·戈文丹博士和他的同事招募了76名接受过标准治疗的局部晚期或转移患者。研究的主要终点是毒性,次要终点是客观反应率、反应持续时间、疾病控制率、无进展生存率和稳定疾病持续时间。
患者分为180毫克、360毫克、720毫克和960毫克四个剂量组,每天口服一次,持续21天,随后进行放射影像学和其他检查。研究第一阶段的初始数据在两个月前的第55届美国临床肿瘤学会年会上发表。这次WCLC大会上公布的是后续的数据,包括了34名NSCLC患者,其中23名患者的疗效可以评估。与今年ASCO年会上公布AMG 510数据相比,WCLC 2019公布的数据纳入了更多数量的患者。
在可评估的患者中有13名接受每日960mg目标剂量,其中7名(54%)在一个或多个时间点达到部分反应,6名(46%)病情稳定,疾病控制率为100%。
34名NSCLC患者均未发生剂量限制毒性和导致停药的不良事件,其中27名患者仍在接受治疗。在34名患者中,只有9名(26.5%)报告了一级或二级治疗相关不良事件(TRAEs),3名患者报告了三级治疗相关的不良反应(贫血和腹泻)。未出现四级及以上不良事件病例。
据悉,FDA已授予AMG 510快速通道资格,用于治疗携带KRAS G12C突变的经治NSCLC患者。
好医友指出,KRAS G12C突变型肺腺癌是NSCLC最大的亚群之一。AMG 510表现出喜人的抗癌活性,这意味着,在不久的将来,这类患者终于有望迎来口服靶向治疗方法。期待该疗法早日获批,造福更多肺癌患者。
想了解更多肺癌新疗法相关信息,欢迎后台留言或致电好医友(400-060-9693)。
2019-09-11 16:46

好医友小编