FDA批准DARZALEX与标准剂联合治疗多发性骨髓瘤
 多发性骨髓瘤
|
阅读量:130次
多发性骨髓瘤
|
阅读量:130次
Janssen Biotech公司宣布,美国FDA已经批准DARZALEX(daratumumab)与 lenalidomide(一种免疫调节剂)和dexamethasone,或者与bortezomib(一种蛋白酶体抑制剂,PI)和dexamethasone用于联合治疗多发性骨髓瘤(multiple myeloma),这些患者至少已经接受过一次先前治疗。临床研究曾表明,与单用lenalidomide和dexamethasone相比,DARZALEX联合lenalidomide和dexamethasone治疗多发性骨髓瘤,先前经治患者的疾病进展或死亡的风险降低了63%(危险比[HR]=0.37; 95%CI [0.27,0.52],p<0.0001)。与单用bortezomib和dexamethasone相比,采用bortezomib、dexamethasone、DARZALEX联合疗法的经治患者的疾病进展或死亡的风险降低了61%(HR=0.39; 95%CI [0.28,0.53],p<0.0001)。Lenalidomide和dexamethasone目前是两种最广泛使用的多发性骨髓瘤标准治疗制剂。

多发性骨髓瘤是一种不可治愈的血癌,源于恶性浆细胞在骨髓中不受控制地生长。2015年全球范围内,估计12.4万多例患者被诊断出患有多发性骨髓瘤,8.7万多名病人死于该疾病。虽然一些多发性骨髓瘤患者没有明显症状,大多数患者由于骨折或骨骼疼痛、低红细胞计数、疲劳、钙含量升高、肾脏问题或感染等症状而被确诊。

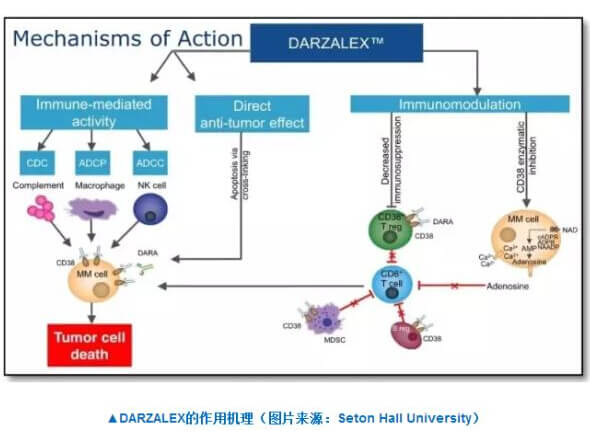
静脉注射用DARZALEX是世界上首个获批的CD38介导的溶细胞性抗体。CD38是一种在多发性骨髓瘤细胞中高表达的细胞表面蛋白。DARZALEX被认为可以通过多种免疫介导的作用机制来诱导肿瘤死亡:包括互补依赖性细胞毒作用(CDC)、抗体依赖性细胞介导的细胞毒作用(ADCC)和抗体依赖性细胞吞噬作用(ADCP)以及通过细胞凋亡(apoptosis)。该药物于2015年11月首次被FDA批准作为部分多发性骨髓瘤患者的单一疗法治疗,他们曾接受过PI或免疫调节剂治疗,或针对PI和免疫调节剂都是难治的。
昨天的批准有来自POLLUX (MMY3003) 和CASTOR (MMY3004) 两个3期研究的积极数据支持。与标准护理方案lenalidomide和dexamethasone治疗相比,加了DARZALEX后治疗方案显著改善无进展生存期(PFS),达到了临床试验的主要终点。这些临床研究的更新数据结果将作为口头报告形式在加州圣地亚哥即将举行的第58届美国血液学会(ASH)年会上得以公布。
该批准是在2016年8月Janssen向FDA提交补充生物制剂许可申请(sBLA)三个月后得以完成的。FDA也曾于2016年7月向DARZALEX授予突破性疗法认定。
“我们为DARZALEX的快速开发和先前批准上市而感到自豪,但我们的工作并不止于此,”Janssen全球肿瘤部门负责人Peter F. Lebowitz博士说道:“我们仅仅刚开始发现这个化合物的全部潜力,我们仍然致力于继续研究daratumumab,以更充分地了解其对多发性骨髓瘤和其他癌症类型患者的临床效益。”
参考资料:
[1] Johnson & Johnson (JNJ) Release: DARZALEX (Daratumumab) Approved By U.S. FDA In Combination With Two Standard Of Care Regimens For The Treatment Of Patients With Multiple Myeloma Who Have Received At Least One Prior Therapy
[2] Johnson & Johnson官方网站
来源:药明康德
2018-11-16 14:52

好医友小编
联系医学顾问
医学顾问微信在线
